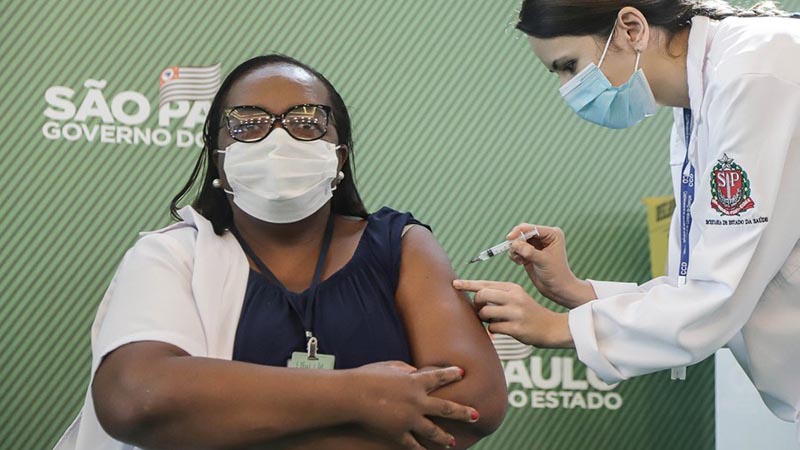
BEIJING, 6 febrero, 2021 (Xinhua) -- Imagen del 23 de diciembre de 2020 de una trabajadora de Sinovac Biotech, una compañía biofarmacéutica china, laborando en el laboratorio de inspección de calidad de vacunas inactivadas contra la COVID-19, en Beijing, capital de China. La Administración Nacional de Productos Médicos de China otorgó el viernes la aprobación condicional de mercado a CoronaVac, una vacuna inactivada contra la COVID-19 desarrollada por Sinovac Biotech, anunció el sábado la compañía. (Xinhua/Zhang Yuwei)
BEIJING, 6 feb (Xinhua) -- La Administración Nacional de Productos Médicos (ANPM) de China otorgó el viernes la aprobación condicional de mercado a CoronaVac, una vacuna inactivada contra la COVID-19 desarrollada por Sinovac Biotech, anunció hoy sábado la compañía.
La vacuna de Sinovac, producida por Sinovac Life Sciences Co. Ltd., afiliada a Sinovac Biotech, fue aprobada para su uso de emergencia en China el pasado mes de junio. La vacuna empezó a utilizarse para la inoculación de emergencia entre algunos grupos especiales del país desde julio del año pasado.
Desde este mes de enero, países como Indonesia, Turquía, Brasil, Chile, Colombia, Uruguay y Laos aprobaron sucesivamente el uso de emergencia de la vacuna Sinovac a nivel local.
Estos países reconocen los resultados de la investigación clínica de la vacuna, considerando que tiene efectos evidentes en la reducción del tratamiento médico, la hospitalización, los casos críticos y las muertes causadas por la COVID-19, y que es de gran importancia para la prevención y el control de la pandemia, dijo Sinovac Biotech mediante un comunicado de prensa en su sitio de internet.
Sinovac Life Sciences Co. Ltd. presentó el 3 de febrero una solicitud para la aprobación condicional de mercado de CoronaVac, que se concedió sobre la base de los ensayos clínicos de fase 3 de la vacuna en el extranjero durante dos meses, indicó.
La ANPM pidió a la empresa que siga realizando los ensayos clínicos pertinentes, cumpla los requisitos condicionales y presente a tiempo los resultados de la investigación de seguimiento.
"Esperamos ofrecer más vacunas seguras y eficaces lo antes posible y ayudar a controlar la COVID-19 en última instancia aumentando las tasas de inoculación, lo que permitirá que el desarrollo social y económico vuelva a la vía normal", señaló Yin Weidong, presidente y director general de Sinovac.
De acuerdo con la empresa, el procedimiento de vacunación incluye dos inyecciones con un intervalo de 14 a 28 días y cada dosis es de 0,5 mililitros.